推荐产品
公司新闻/正文
「青莲客户文献」蛋白组学与微生物多样性测序联合分析揭示治疗溃疡性结肠炎新靶点
人阅读 发布时间:2022-01-24 10:19

青莲客户致谢文章又来啦~ 2021年10月21日来自中国医学科学院生物医学工程研究所刘天军团队在Frontiers in Pharmacology上发表题为“Photodynamic Therapy of Novel Photosensitizer Ameliorates TNBS-Induced Ulcerative Colitis via Inhibition of AOC1”研究论文。
利用新型光敏剂的光动力学疗法通过抑制AOC1 改善 2,4,6-(TNBS)诱导的溃疡性结肠炎。
溃疡性结肠炎(UC)是一种病因尚不十分清楚的慢性、非特异性炎症性疾病。病变局限于大肠黏膜及黏膜下层,多位于乙状结肠和直肠,呈连续的非节段性分布。UC具有病变广泛、发病机制复杂、频繁复发和易癌变等特征,已被世界卫生组织(WHO)列入现代难治性疾病清单。寻找一种有效的UC治疗方法已成为临床实践中的一个关键科学问题。

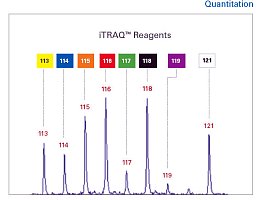
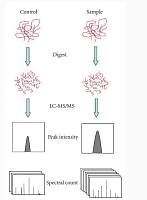
光动力疗法(Photodynamic therapy,PDT)作为一种有前途的理化治疗方法,作者利用新型光敏剂LD4对UC大鼠模型进行治疗,探讨其治疗效果及作用机制。通过微生物多样性测序和定量蛋白质组学分析(均由青莲百奥提供服务)表明新型光敏剂 LD4-PDT 代表了UC的有效治疗方法,蛋白质组学分析结果显示AOC1可能是有希望的靶标。
实验结果
1、LD4-PDT对TNBS诱导的UC模型大鼠结肠组织的蛋白谱进行了重编程
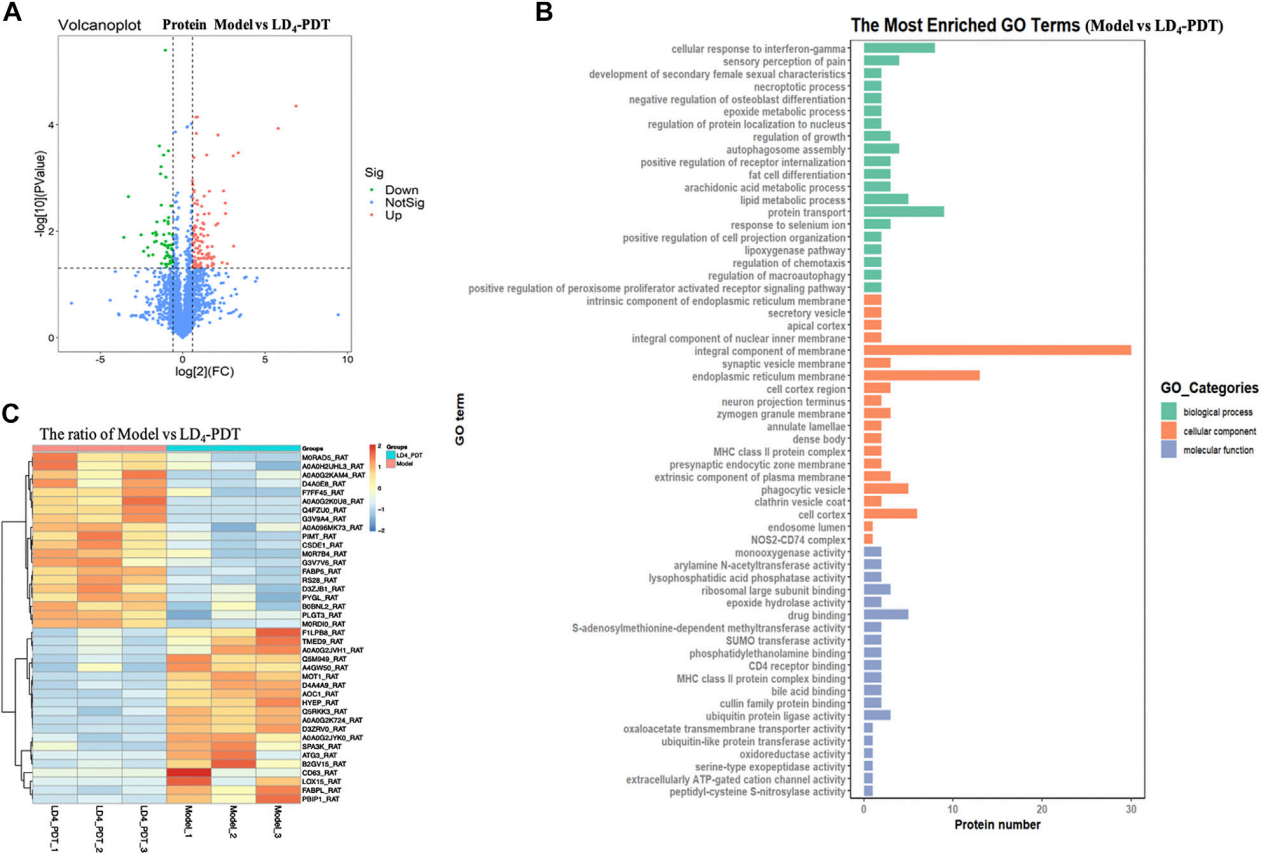
为了研究 LD4-PDT 治疗 UC 的机制,作者利用非标记定量蛋白质组学分析UC模型大鼠结肠组织(对照组,TNBS模型组和 LD4-PDT 治疗组)中的蛋白谱。通过蛋白差异分析及GO分析表明用 LD4-PDT 处理改变了结肠蛋白表达谱(图1)。细胞组分分析表明LD4-PDT 处理导致了细胞皮层、胞内细胞器和主要组织相容性复合体 II 类蛋白的变化。分子功能分析发现LD4-PDT 处理改变了加氧酶和水解酶的活性。
通过热图筛选了40 种显著差异表达的蛋白,结果表明模型组AOC1的表达显著上调,而这种上调在 LD4-PDT 治疗后被消除。AOC1在免疫细胞运输中的作用使其成为自身免疫性疾病和炎症性疾病的靶点,因此作者选择AOC1做进一步研究。
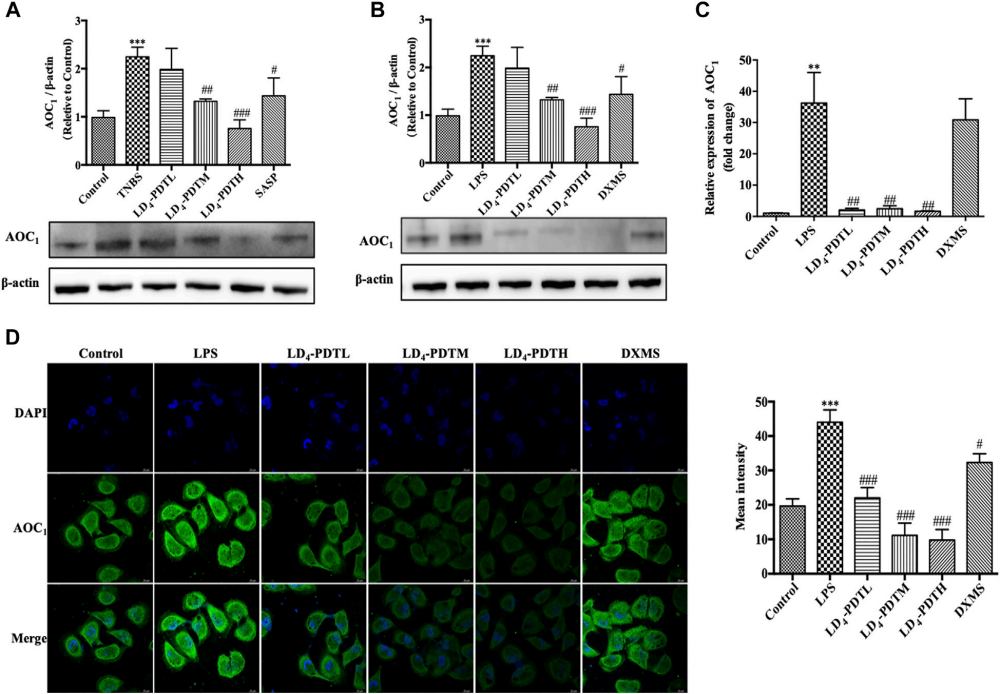
2、LD4-PDT通过抑制AOC1保护肠道
蛋白印迹法进一步验证AOC1的蛋白的表达,与对照组相比,TNBS模型组AOC1表达显著增加,LD4-PDT 治疗后 AOC1表达显著降低。此外用Western Blot、 qRT-PCR 和免疫荧光检测AOC1在HCoEpiC细胞中的表达,与动物实验结果一致(图2)。作者对HCoEpiC 细胞中的AOC1基因进行敲低及过表达,结果进一步表明 LD4-PDT治疗可能通过抑制 AOC1介导的AKT/IKK/NF-κB通路发挥作用,因此,通过 LD4-PDT治疗或其他方法敲除AOC1蛋白均可缓解UC症状。
3、LD4-PDT重塑了TNBS诱导的UC模型大鼠的肠道细菌组成模式
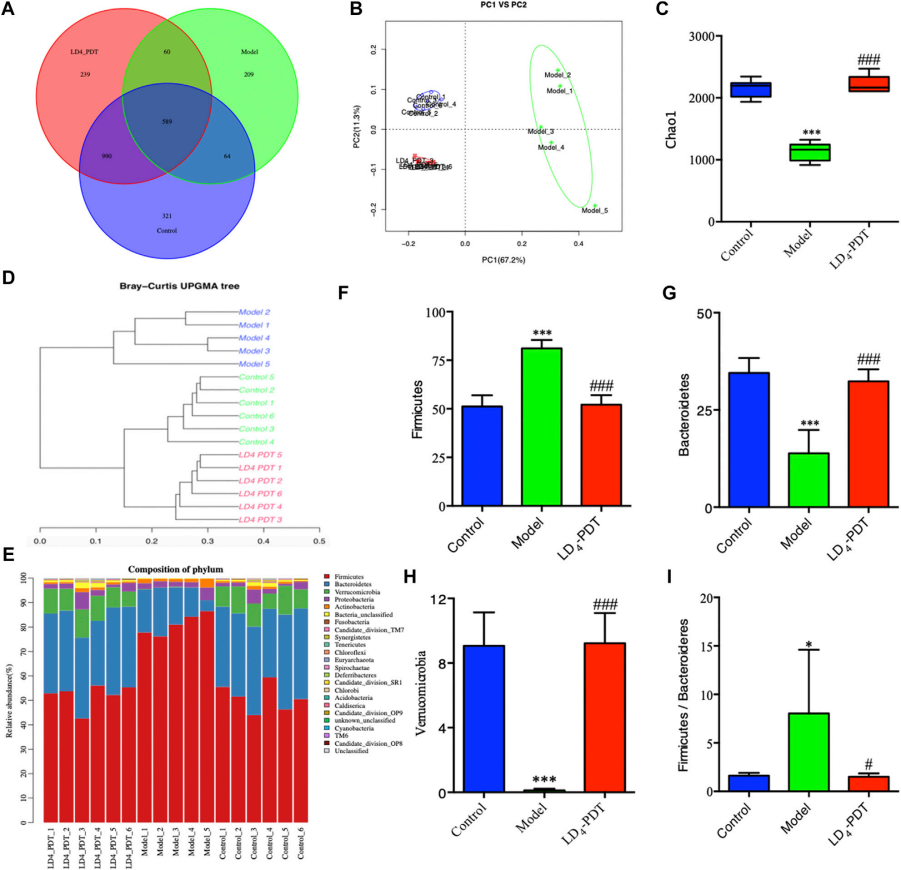
图3:LD4-PDT治疗改变了TNBS诱导的UC模型大鼠的肠道微生物群
综上所述,作者发现LD4-PDT 治疗可促进结肠粘膜愈合,调节肠道菌群,改善UC临床症状。LD4-PDT可以减少由AOC1介导的粘膜炎症反应,最后确定AOC1是UC干预的潜在靶点。新型光敏剂LD4是一种有效的PDT治疗UC的候选药物。
题目:新型光敏剂的光动力学疗法通过抑制AOC1 改善 TNBS诱导的溃疡性结肠炎
期刊名称:Frontiers in Pharmacology
影响因子:4.225
组学技术:16s rRNA测序、非标记定量蛋白组学