推荐产品
公司新闻/正文
「青莲聚焦」新策略:单细胞也可以多组学同时分析啦
人阅读 发布时间:2021-12-20 09:52

近日,国家蛋白质中心的(北京)秦伟捷研究员团队在Analytical Chemistry上发表“An Integrated Strategy for Mass Spectrometry-Based Multiomics Analysis of Single Cells”。研究人员开发了一种微孔芯片,并对其表面进行了亲水处理,可以串联完成代谢物和蛋白质的提取以及蛋白酶切工作,产物可以直接进行单细胞代谢物质谱检测,并在不进行磷酸化肽富集的情况下同时进行蛋白质组分析和磷酸化蛋白质组分析,结果共鉴定到132个注释代谢物,1200多种蛋白质和大规模的单细胞磷酸化分析数据集。
芯片的硅孔表面结合Oligo-EG分子,将获得的细胞分布于每个微孔中,然后使用80% 预冷的乙腈进行代谢物的提取,同时,蛋白也会结合在Oligo-EG分子修饰的孔内表面。收集提取的代谢物直接进行质谱分析,蛋白继续进行在微孔内进行酶切、消化、收集肽段进行质谱检测。研究人员采用DIA-MS方法同时进行单细胞全蛋白质组分析和磷酸化蛋白质组分析。

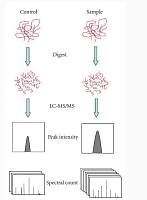
图1:基于HILIC的代谢物和蛋白质串联提取示意图及基于质谱的单细胞多组学分析的综合策略
研究人员分析了不同样本之间的相关性,无论是蛋白水平还是肽段水平,相关性系数均在0.95左右,表示该技术体系非常稳定。单细胞蛋白组的DIA实验中在50个和1个HT22细胞中,分别鉴定到约3488和1389个蛋白,磷酸化肽段分别约1945和535条(n=6),同时可以看到作为空白对照的样本只鉴定到50个以下的蛋白。以上结果均表明本研究方法能很好地适用于单细胞蛋白和磷酸化肽段的鉴定。

图2:微孔-HILIC串联提取及DIA质谱分析的可重复性((a)蛋白和(b)多肽)
为了进一步探索作者提出的策略是否有能力分析单细胞蛋白之间的差异,研究人员利用微孔芯片对诺考达唑处理和未处理的共36个HT22细胞进行质谱分析,共鉴定了1594 个蛋白和1728个磷酸化肽段。PCA结果显示本次单细胞DIA的蛋白和磷酸化肽段的定量数据均能非常好地将两组对照样本区分开,且筛选出的164个差异蛋白中包含很多与诺考达唑作用机制密切相关的蛋白(Stag2, Actn1, Dstn, and Ndel1等)。结果表明该策略可以在单细胞水平上表征药物干扰的影响。研究人员还分析了代谢组学PCA结果显示根据诺考达唑处理后的这些细胞是聚集的。说明该策略使用三种组学数据中的任何一种均可以在单细胞水平上区分不同的细胞状态。

图3:经过和未经过诺考达唑处理的单细胞中鉴定到的蛋白(a)和磷酸化肽(b)的PCA分析
文献证明了该策略的高稳定性以及可重复性,而且这种多组学的分析策略可能会在细胞异质性中得到广泛的应用。青莲百奥的单细胞蛋白质组学正是基于文献中的研究策略,利用微孔芯片技术结合质谱分析,突破蛋白质无法扩增以及单个细胞蛋白样本微量的难题,实现高灵敏度、高覆盖度的单细胞蛋白检测结果,同时在不富集磷酸化修饰肽段的前提下仍能检测大量磷酸化修饰肽段。随着基于单细胞蛋白质组学质谱研究方法的不断发展,相信单细胞蛋白组以及单细胞多组学分析在临床诊断、疾病分型以及细胞发展机制这些重大生命科学领域方面的应用将会越来越广泛。